照合元データの構造の違いによるトラブル
投稿日:2020.06.25
更新日:2024.07.31
照合元データのトラブル
こんにちは、営業のNです。
一度は新記載添付文書の作成依頼が増えたかと思いましたが、また減少してきたような気がします。
来年8月以降に、添付文書同梱廃止・電子化が控えていますので、それまで改版を待とう、という判断が働いているのかもしれません。
一方で5年間の猶予期間に沿ったスケジュールを決めて着実に進めておられる製薬会社様もあります。
間際になるとマンパワーの問題もでてきますので、早めの着手お願いいたします。
照合元データによるトラブル事例
さて、今回も実際にXMLを作成したときにおこったトラブルについてご紹介したいと思います。
今回は(今回も?)相当マニアックな事例です。
「照合元データの改訂記号の位置がおかしかったので、修正をかけたら自動受理されなかった」という事例です 。
一般的には改訂記号の位置は、自動受理には影響しません。
しかし、場合によっては自動受理されないときもあるようです。
そちらについてご説明します。
トラブル内容
今回問題になった照合元データは下記です。
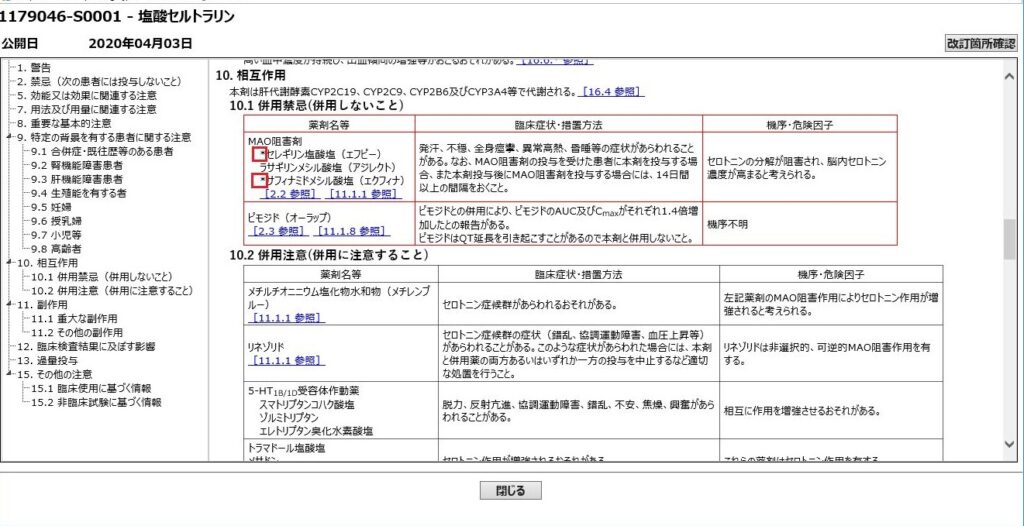
□をご覧になればわかるとおり、「セレギリン塩酸塩」と「サフィナミドメシル酸塩」の前に改訂記号がついています。
しかし、実はこちらの照合元データはミスがあります。
「セレギリン塩酸塩」でなくて、「ラサリギンメシル酸塩」が改訂記号がつくべき対象でした。
(なぜこうなったかは後述します)
こちらのジェネリック品の添付文書を作成するために照合元データをとりこみました。
取り込んでみたところ、改訂記号の位置が違うので修正しました。
データを提出し、通常ならば改訂記号の位置は自動受理には影響しないので自動受理されるはずです。
しかし、なぜか今回はエラーになってしまいました。
●照合元データのソースをみてみます
なぜでしょうか?照合元データのソースをみてみたら理由がわかりました。
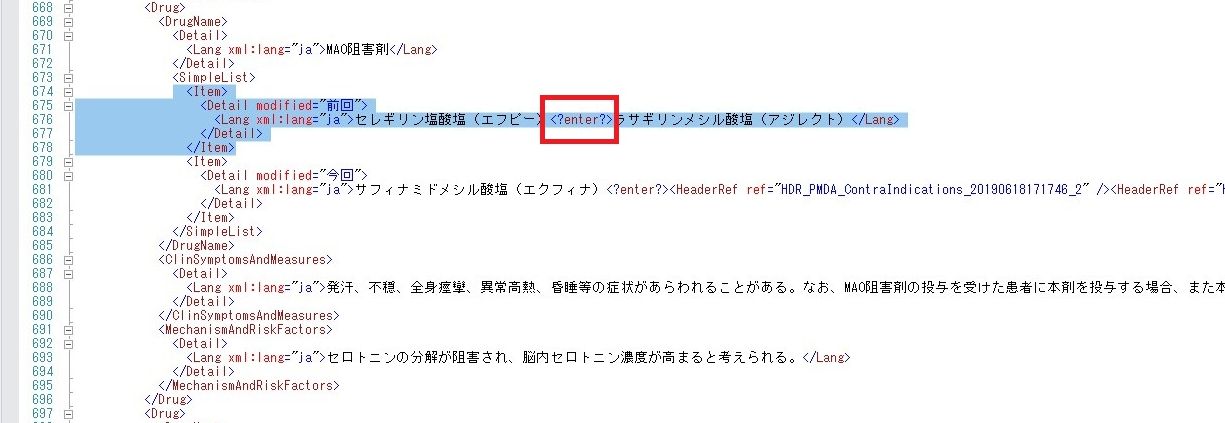
□部分です。強制改行<?enter?>がかかっていました。
本来「 *」をつけたかった「ラサリギンメシル酸塩」に、「*」がつかなかったのもこのせいです。
ただしくはこちらのソースだと思います。今回はじめに提出したのもこちらのソースです。

改訂記号の位置は自動受理に影響しないといえども、このように文章構造がちがったら自動受理はしてもらえないようです。
見た目ではわからないところがこの問題の厄介なところです。
●先発薬を見てみます
さて、今回、照合元データがおかしくなった理由を推測してみます。
こちらの先発品では改訂記号はこのような表現になっています。

ご覧になりましたように、薬剤単位でなくて、「MAO阻害薬」という上位単位で改訂記号がついています。
しかし、「新記載要領に基づく添付文書等の作成の留意点(Q&A)について」のNo.18に下記のような記述があります。
ただし、下位の項目を全て新設した場合は、それらを包含する上位の項目番号の前に「*」又は「**」を付すこと。
表形式で記載する「10.1 併用禁忌」、「10.2 併用注意」及び「11.2 その他の副作用」においては、最左欄の事象名又は薬剤名の前に「*」又は「**」を付すこと。
該当する項目名及び項目番号ごと削除した場合は改訂箇所の表示は要さないこと。
つまりは、「10.1併用禁忌」では、薬剤単位に改訂記号をつけることが推奨されています。
「MAO阻害薬」という単位は薬剤単位になるのかどうかはわかりません。先発薬メーカーさまは薬剤単位と理解してこの位置に付したのだと思います。
しかし、照合元データを作成するときには、「薬剤単位」の理解が異なり、改訂記号をつける位置のレベルをひとつ落としたのでしょう。
その際に強制改行タグ<?enter?>が邪魔をして想定と違うところに改訂記号がはいったのだと思われます。
本ブログは特定の製品などを誹謗する目的ではなく、皆様のXML作成を手助けし
ひいては製薬業界の情報提供活動に寄与する目的で記載しております。











